Pasteurisasi, Desinfeksi, dan Sterilisasi
1. PASTEURISASI
Pasteurisasi
adalah proses pemanasan makanan, biasanya cair, dengan suhu tertentu untuk
jangka waktu tertentu, dan kemudian pendinginan segera. Proses ini memperlambat
pertumbuhan mikroba dalam makanan. Proses pemanasan anggur untuk tujuan
pelestarian telah dikenal di Cina sejak 1117 dan didokumentasikan di Jepang
pada tahun 1568 dalam buku harian Tamonin-nikki, tapi versi modern diciptakan
oleh kimiawan Perancis dan mikrobiologi Louis Pasteur.
Tes pasteurisasi pertama diselesaikan oleh Louis Pasteur dan Claude Bernard pada bulan April 1862. Proses pada awalnya dipahami sebagai cara untuk mencegah anggur dan bir dari souring.
Tes pasteurisasi pertama diselesaikan oleh Louis Pasteur dan Claude Bernard pada bulan April 1862. Proses pada awalnya dipahami sebagai cara untuk mencegah anggur dan bir dari souring.
Tidak seperti
sterilisasi, pasteurisasi tidak dimaksudkan untuk membunuh semua
mikro-organisme dalam makanan. Sebaliknya pasteurisasi bertujuan untuk
mengurangi jumlah patogen yang layak sehingga mereka tidak menyebabkan penyakit
(dengan asumsi produk yang dipasteurisasi disimpan sebagai ditunjukkan dan
dikonsumsi sebelum tanggal kedaluwarsa).
Skala komersial sterilisasi makanan tidak umum karena hal itu merugikan mempengaruhi rasa dan kualitas produk. Produk makanan tertentu, seperti produk susu, yang dipanaskan untuk memastikan mikroba patogen dihancurkan.
Skala komersial sterilisasi makanan tidak umum karena hal itu merugikan mempengaruhi rasa dan kualitas produk. Produk makanan tertentu, seperti produk susu, yang dipanaskan untuk memastikan mikroba patogen dihancurkan.
Proses
pasteurisasi merupakan proses pemanasan dengan suhu yang relatif cukup rendah
(dibawah 1000C) dengan tujuan untuk menginaktifasi enzim dan
membunuh mikroba pembusuk. Pemilihan proses ini didasarkan pada sifat produk
yang relatif asam sehingga mikroba menjadi lebih sensitif terhadap panas.
Selain itu, penggunaan panas yang tidak terlalu tinggi juga dapat mengurangi
resiko rusaknya beberapa zat gizi seperti vitamin C.
Proses pasteurisasi sedikit memperpanjang umur simpan produk pangan dengan cara membunuh semua mikroorganisme patogen (penyebab penyakit) dan sebagian besar mikroorganisme pembusuk, melalui proses pemanasan. Karena tidak semua mikroorganisme pembusuk mati oleh proses pasteurisasi, maka untuk memperpanjang umur simpannya produk yang telah dipasteurisasi biasanya disimpan di refrigerasi (suhu rendah).
Proses pasteurisasi dapat dilakukan dengan beberapa cara, dengan cara tidak kontinyu (batch) dan kontinyu. Pasteurisasi secara batch dilakukan dengan memanaskan bahan pangan pada suhu dan waktu pasteurisasi tertentu, selanjutnya dikemas dalam kemasan steril dengan teknik pengisian hot filling.
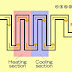
Sementara pasteurisasi kontinyu dilakukan dengan menggunakan pelat pemindah panas (plate heat exchanger). Proses berlangsung tanpa terputus: bahan yang telah dipasteurisasi langsung dibawa ke tahap pendinginan dan langsung dikemas.
Cara kontinyu menggunakan suhu yang lebih tinggi dengan waktu proses yang lebih singkat dibandingkan metode batch. Proses sterilisasi menggunakan kombinasi suhu tinggi dan waktu tertentu untuk membunuh semua mikroorganisme termasuk sporanya didalam bahan pangan, yang dapat tumbuh pada kondisi normal.
Proses ini lebih intens dari proses pasteurisasi, menggunakan suhu di atas 1000C dengan waktu yang lebih lama sehingga bisa mempengaruhi penampakan dan rasa produk. Sterilisasi komersial tidak sama dengan sterilisasi absolut. Pada sterilisasi komersial, proses sterilisasi ditujukan untuk membunuh semua mikroorganisme yang hidup pada suhu penyimpanan normal (disuhu ruang).
Proses pasteurisasi sedikit memperpanjang umur simpan produk pangan dengan cara membunuh semua mikroorganisme patogen (penyebab penyakit) dan sebagian besar mikroorganisme pembusuk, melalui proses pemanasan. Karena tidak semua mikroorganisme pembusuk mati oleh proses pasteurisasi, maka untuk memperpanjang umur simpannya produk yang telah dipasteurisasi biasanya disimpan di refrigerasi (suhu rendah).
Proses pasteurisasi dapat dilakukan dengan beberapa cara, dengan cara tidak kontinyu (batch) dan kontinyu. Pasteurisasi secara batch dilakukan dengan memanaskan bahan pangan pada suhu dan waktu pasteurisasi tertentu, selanjutnya dikemas dalam kemasan steril dengan teknik pengisian hot filling.
Sementara pasteurisasi kontinyu dilakukan dengan menggunakan pelat pemindah panas (plate heat exchanger). Proses berlangsung tanpa terputus: bahan yang telah dipasteurisasi langsung dibawa ke tahap pendinginan dan langsung dikemas.
Cara kontinyu menggunakan suhu yang lebih tinggi dengan waktu proses yang lebih singkat dibandingkan metode batch. Proses sterilisasi menggunakan kombinasi suhu tinggi dan waktu tertentu untuk membunuh semua mikroorganisme termasuk sporanya didalam bahan pangan, yang dapat tumbuh pada kondisi normal.
Proses ini lebih intens dari proses pasteurisasi, menggunakan suhu di atas 1000C dengan waktu yang lebih lama sehingga bisa mempengaruhi penampakan dan rasa produk. Sterilisasi komersial tidak sama dengan sterilisasi absolut. Pada sterilisasi komersial, proses sterilisasi ditujukan untuk membunuh semua mikroorganisme yang hidup pada suhu penyimpanan normal (disuhu ruang).
Harus diingat,
bahwa beberapa mikroorganisme bisa membentuk spora yang mampu bertahan pada
suhu tinggi. Pada kondisi penyimpanan yang benar, spora ini tidak bergerminasi,
tetapi pada suhu penyimpanan yang salah (suhu penyimpanan diatas suhu
penyimpanan normal), maka spora tersebut dapat bergerminasi dan menyebabkan
kerusakan makanan kaleng.
Clostridium botulinum menjadi target utama dari proses sterilisasi komersial untuk pangan yang pHnya diatas 6.4, atau awnya diatas 85%. Ketidakcukupan proses sterilisasi (suhu tidak tercapai atau waktu sterilisasi kurang) akan menyebabkan spora C. botulinum bergerminasi dan tumbuh serta memproduksi toksin botulin yang sangat mematikan didalam makanan kaleng tersebut.
Waktu dan suhu sterilisasi bahan pangan tergantung pada jenis wadah yang digunakan, dan kondisi (jenis, komposisi dan kekentalan) bahan pangan yang akan disterilisasi.
Sebagai contoh, proses sterilisasi soup memerlukan waktu yang lebih pendek dari proses sterilisasi kornet. Cairan (kuah) soup akan membantu mempercepat proses pindah panas (heat transfer) secara konveksi.
Pada sterilisasi kornet, proses pindah panas terjadi secara konduksi sehingga proses pemanasan berjalan lambat.
Produk pangan sterilisasi mempunyai umur simpan yang panjang dan dapat disimpan pada suhu ruang, misalnya kornet dan cocktail buah kalengan. Produk juga harus dilengkapi dengan keterangan tanggal kadaluarsa pada labelnya.
Clostridium botulinum menjadi target utama dari proses sterilisasi komersial untuk pangan yang pHnya diatas 6.4, atau awnya diatas 85%. Ketidakcukupan proses sterilisasi (suhu tidak tercapai atau waktu sterilisasi kurang) akan menyebabkan spora C. botulinum bergerminasi dan tumbuh serta memproduksi toksin botulin yang sangat mematikan didalam makanan kaleng tersebut.
Waktu dan suhu sterilisasi bahan pangan tergantung pada jenis wadah yang digunakan, dan kondisi (jenis, komposisi dan kekentalan) bahan pangan yang akan disterilisasi.
Sebagai contoh, proses sterilisasi soup memerlukan waktu yang lebih pendek dari proses sterilisasi kornet. Cairan (kuah) soup akan membantu mempercepat proses pindah panas (heat transfer) secara konveksi.
Pada sterilisasi kornet, proses pindah panas terjadi secara konduksi sehingga proses pemanasan berjalan lambat.
Produk pangan sterilisasi mempunyai umur simpan yang panjang dan dapat disimpan pada suhu ruang, misalnya kornet dan cocktail buah kalengan. Produk juga harus dilengkapi dengan keterangan tanggal kadaluarsa pada labelnya.
1.1.Tujuan dan Metode
Pasteurisasi
Pasteurisasi tidak mematikan semua mikroorganisme,
tetapi hanya yang bersifat patogen dan tidak membentuk spora. Oleh sebab itu,
proses ini sering diikuti dengan teknik lain misalnya pendinginan atau
pemberian suhu. Pasteurisasi memiliki tujuan :
a)
Untuk membunuh
bakteri patogen, yaitu bakteri yang berbahaya karena dapat menimbulkan penyakit
pada manusia. Bakteri pada susu yang bersifat patogen misalnya mycobacterium
tuberculosis dan coxiella bunetti, dan mengurangi populasi
bakteri.
b)
Untuk memperpanjang
daya simpan alat-alat medis.
c)
Dapat menimbulkan
citarasa yang lebih baik pada produk susu.
d)
Pada susu proses
ini dapat meng-in active-kan enzim fosfatase dan katalase yaitu enzim
yang membuat susu cepat rusak.
Metode pasteurisasi yang umum digunakan adalah
pasteurisasi dengan suhu tinggi dan waktu singkat (High Temperature Short
Time, HTST), yaitu proses pemanasan susu selama 15 – 16 detik pada suhu
71,7 – 75 °C dengan alat Plate Heat Exchanger. Pasteurisasi dengan suhu
rendah dan waktu lama (Low Temperature Long Time, LTLT), yakni proses pemanasan
susu pada suhu 61 °C selama 30 menit.
Pasteurisasi dengan suhu sangat tinggi (Ultra High Temperature) yaitu memnaskan susu pada suhu 1310C selama 0,5 detik. Pemanasan dilakukan dengan tekanan tinggi untuk menghasilkan perputaran dan mencegah terjadinya pembakaran susu pada alat pemanas.
Pasteurisasi dengan suhu sangat tinggi (Ultra High Temperature) yaitu memnaskan susu pada suhu 1310C selama 0,5 detik. Pemanasan dilakukan dengan tekanan tinggi untuk menghasilkan perputaran dan mencegah terjadinya pembakaran susu pada alat pemanas.
Pasteurisasi dengan suhu tinggi dan waktu lama (High Temperature Long
Time, HTLT) dilakukan dengan cara pemanasan alat-alat medis selama 20 menit
pada temperatur 85 – 100 °C dengan menggunakan pemanas (heater). Sedangkan
pasteurisasi dengan temperatur rendah dan waktu lama (Low Temperature Long
Time, LTLT) dilakukan dengan cara proses pemanasan alat – alat medis pada
temperatur kurang dari 85 °C selama 10 menit.
1.2.Pasteurisasi susu
Pasteurisasi biasanya terkait dengan susu.
Pasteurisasi (yaitu, panas dan tegang) krim untuk meningkatkan kualitas menjaga
mentega dipraktekkan di Inggris sebelum 1773 dan telah diperkenalkan ke Boston,
New England, oleh 1773, meskipun tidak secara luas dipraktekkan di AS untuk dua
puluh tahun ke depan. Masih ditulis sebagai sebuah proses baru di surat kabar
Amerika sebagai sebagai akhir 1802.
Pasteurisasi susu disarankan oleh Franz von Soxhlet
pada tahun 1886 . Ini adalah alasan utama untuk kehidupan rak diperpanjang
susu. Suhu Tinggi Waktu Pendek (HTST) pasteurisasi susu biasanya memiliki
kehidupan rak berpendingin dua sampai tiga minggu, sedangkan ultra-pasteurisasi
susu dapat bertahan lebih lama, kadang-kadang dua sampai tiga bulan.
Ketika ultra-perlakuan panas (UHT) yang dikombinasikan dengan penanganan kontainer steril dan teknologi (seperti kemasan aseptik), bahkan dapat disimpan selama 6-9 bulan unrefrigerated
Ketika ultra-perlakuan panas (UHT) yang dikombinasikan dengan penanganan kontainer steril dan teknologi (seperti kemasan aseptik), bahkan dapat disimpan selama 6-9 bulan unrefrigerated
Susu pasteurisasi adalah susu segar yang telah mengalami pemanasan pada
suhu di bawah 100oC. Standar pasteurisasi menggunakan suhu 62oC
selama 3 menit atau suhu 71oC selama 15 detik. Pemanasan tersebut
bertujuan mematikan bakteri – bakteri patogen, sehingga susu pasteurisasi dalam
jangka waktu tertentu aman untuk diminum tanpa harus dipanaskan lagi. Pada
penyimpanan dingin ± 4oC, susu pasteurisasi tidak rusak dalam waktu
± 7 hari (Hadiwiyoto, 1994).
2.
DISINFEKTAN
Disinfektan adalah bahan kimia yang digunakan untuk mencegah
terjadinya infeksi
atau pencemaran oleh jasad renik
atau obat untuk membasmi kuman penyakit. Pengertian lain dari disinfektan adalah senyawa kimia yang bersifat
toksik dan memiliki kemampuan membunuh mikroorganisme yang terpapar secara langsung oleh disinfektan.
Disinfektan tidak memiliki daya penetrasi sehingga tidak mampu membunuh mikroorganisme yang terdapat di dalam celah atau cemaran mineral. Selain itu disinfektan tidak dapat membunuh spora bakteri sehingga dibutuhkan metode lain seperti sterilisasi dengan autoklaf.
Disinfektan tidak memiliki daya penetrasi sehingga tidak mampu membunuh mikroorganisme yang terdapat di dalam celah atau cemaran mineral. Selain itu disinfektan tidak dapat membunuh spora bakteri sehingga dibutuhkan metode lain seperti sterilisasi dengan autoklaf.
Efektivitas disinfektan dipengaruhi oleh beberapa faktor,
diantaranya lama paparan, suhu,
konsentrasi disinfektan, pH, dan ada tidaknya
bahan pengganggu. pH merupakan faktor penting dalam menentukan efektivitas
disinfektan, misalnya saja senyawa klorin akan kehilangan aktivitas
disinfeksinya pada pH lingkungan lebih dari 10. Contoh senyawa pengganggu yang
dapat menurunkan efektivitas disinfektan adalah senyawa organik.
Syarat
ideal suatu disinfektan yaitu :
- Bekerja cepat, efektif, broad spektrum (bakteri, virus dan jamur)
- Aktivitas tidak dipengaruhi bahan organik, suhu, pH, kesadahan air dan detergen
- Punya efek residual yang baik
- Tidak toksik pada hewan dan manusia
- Non korosif, non staining dan baunya disukai (beraroma)
- Stabil dalam penyimpanan setelah dipakai
- Terbiodegradasi / ramah lingkungan
- Mudah diaplikasikan, tersedia dan ekonomis.
2.1.Penggunaan Desinfektan
Desinfektan sangat penting bagi rumah sakit dan klinik. Desinfektan akan
membantu mencegah infeksi terhadap pasien yang berasal dari peralatan maupun
dari staf medis yang ada di rumah sakit dan juga membantu mencegah tertularnya
tenaga medis oleh penyakit pasien. Perlu diperhatikan bahwa desinfektan harus
digunakan secara tepat (Imbang, 2009).
a. Desinfektan tingkat rendah dapat dibagi menjadi 2
golongan :
Golongan
pertama
- Klorhexidine (Hibitane, Savlon).
- Cetrimide (Cetavlon, Savlon).
- Fenol-fenol (Dettol).
Desinfektan golongan ini tidak aman untuk digunakan :
- Membersihkan cairan tubuh (darah, feses, urin dan dahak).
- Membersihkan peralatan yang terkena cairan tubuh misalnya sarung tangan yang terkena darah.
- Klorheksidine dan cetrimide dapat digunakan sebagai desinfekan kulit
- fenol-fenol dapat digunakan untuk membersihkan lantai dan perabot seperti meja dan almari namun penggunaan air dan sabun sudah dianggap memadai.
Golongan kedua
a). Desinfektan yang melepaskan klorin.
Contoh : Natrium hipoklorit (pemutih,
eau de javel), Kloramin (Natrium tosilkloramid, Kloramin T) Natrium Dikloro
isosianurat (NaDDC), Kalsium hipoklorit (soda terklorinasi, bubuk pemutih)
b). Desinfektan yang melepaskan Iodine misalnya :
Povidone Iodine (Betadine, Iodine lemah)
- Alkohol : Isopropil alkohol, spiritus termetilasi, etanol.
- Aldehid : formaldehid (formalin), glutaraldehid (cidex).
- Golongan lain misalnya : Virkon dan H2O2. (Imbang, 2009)
2.2.Jenis – Jenis Disinfektan
2.2.1.
Golongan
Aldehyde
Sebagai desinfektan glutaraldehid membutuhkan
konsentrasi 1-2%, aktif terhadap bakteri, virus dan jamur, bila waktu kontak
cukup dapat membunuh spora bakteri. Tidak nyaman digunakan karena uapnya cukup
beracun dapat mengiritasi mata, hidung dan tenggorokan, hal ini dapat
menyebabkan gejala asma pada orang yang sensitif.
Cara Kerjanya :
Ø Alkilasi membran dan inti sel memberikan gugus alkil pada
senyawa yang diserang sehingga senyawa tersebut mengalami kerusakan
Ø Pada membran sel glutaraldehid menyerang gugus amin (-NH)
& gugus thiol (-SH) sehingga struktur membran sel rusak
Ø Pada inti sel glutaraldehid merusak atom Nitrogen (N)
pada cincin basa purin pembentuk asam inti.
2.2.2. Formaldehida
Formaldehida atau
dikenal juga sebagai formalin, dengan konsentasi efektif sekitar 8%.
Formaldehida merupakan disinfektan yang bersifat karsinogenik pada
konsentrasi tinggi namun tidak korosif terhadap metal, dapat menyebabkan
iritasi pada mata, kulit, dan pernapasan. Senyawa ini memiliki daya inaktivasi mikroba
dengan spektrum luas. Formaldehida juga dapat terinaktivasi oleh senyawa
organik.
Formaldehida
merupakan senyawa organik dengan rumus CH2O. Ini adalah aldehida
yang paling sederhana, maka nama IUPAC-nya metanal. Formaldehida adalah gas
tidak berwarna dengan bau menyengat yang khas. Ini merupakan prekursor penting
bagi banyak senyawa kimia lainnya, terutama untuk polimer.
Pada tahun 2005, produksi tahunan dunia formaldehida diperkirakan 23 juta ton (£ 50000000000) solusi Komersial formaldehida dalam air, biasa disebut formalin, yang sebelumnya digunakan sebagai disinfektan dan untuk pengawetan spesimen biologis..
Pada tahun 2005, produksi tahunan dunia formaldehida diperkirakan 23 juta ton (£ 50000000000) solusi Komersial formaldehida dalam air, biasa disebut formalin, yang sebelumnya digunakan sebagai disinfektan dan untuk pengawetan spesimen biologis..
Dalam pandangan
luas toksisitas, penggunaan dan volatilitas, paparan formaldehid adalah
pertimbangan signifikan bagi kesehatan manusia. Pada tanggal 10 Juni 2011,
Program Toksikologi Nasional AS telah digambarkan formaldehida sebagai
"dikenal sebagai karsinogen manusia".
2.2.3. Phenol
Phenol
murni sebagai antiseptik sudah tidak dipakai lagi, penggunaan sebagai
desinfektan masih dipertahankan. Derivatnya adalah Chlorinated cresols,
Phenolmercuric compounds. Penggunaan sebagai desinfektan mulai dibatasi karena
bersifat sitotoksik juga terhadap sel mamalia.
Desinfektan phenol digunakan utk mendekontaminasi permukaan kasar dirumah sakit dan laboratorium, penetasan dan farm besar. Tidak dianjurkan pada ruangan anak-anak, penggunaan dikaitkan dengan kasus hiperbilirubinemia
Desinfektan phenol digunakan utk mendekontaminasi permukaan kasar dirumah sakit dan laboratorium, penetasan dan farm besar. Tidak dianjurkan pada ruangan anak-anak, penggunaan dikaitkan dengan kasus hiperbilirubinemia
Cara
kerja senyawa phenol : dengan cara mengganggu dinding sel, menyebabkan
denaturasi protein pada membran dan sitoplasma, serta menonaktifkan
enzim-enzim. Akibatnya protein-protein sel akan menggumpal dan tidak berfungsi
sehingga menyebabkan kematian sel.
Fenol merupakan bahan antibakteri yang cukup kuat dalam
konsentrasi 1-2% dalam air, umumnya dikenal dengan lisol dan kreolin.
Fenol dapat diperoleh melalui distilasi produk minyak bumi tertentu. Fenol bersifat toksik, stabil, tahan lama, berbau tidak sedap, dan dapat menyebabkan iritasi, Mekanisme kerja senyawa ini adalah dengan penghancuran dinding sel dan presipitasi (pengendapan) protein sel dari mikroorganisme sehingga terjadi koagulasi dan kegagalan fungsi pada mikroorganisme tersebut.
Fenol dapat diperoleh melalui distilasi produk minyak bumi tertentu. Fenol bersifat toksik, stabil, tahan lama, berbau tidak sedap, dan dapat menyebabkan iritasi, Mekanisme kerja senyawa ini adalah dengan penghancuran dinding sel dan presipitasi (pengendapan) protein sel dari mikroorganisme sehingga terjadi koagulasi dan kegagalan fungsi pada mikroorganisme tersebut.
2.2.4.
Quats
Adanya
aktivitas quats struktur membran sel terganggu dan menjadi tidak selektif lagi.
Membran sel tidak dapat menahan masuknya racun-racun dari luar sel, begitu pula
komponen penting dari dalam sel akan keluar, akhirnya sel mengalami kematian.
Keuntungan.
·
Broad spektrum
untuk bakteri dan virus
·
Tidak berwarna,
tidak bau, non korosif, non volatil, punya efek residu yang baik, non
toksisitas, non staining, non bleaching, menghasilkan iritasi minimum.
·
Terbiodegradasi
dengan baik, range pH luas (2-12), aman untuk sanitasi air minum unggas
(40-100ppm), tidak dipengaruhi oleh suhu, baik digunakan pada air sadah, mudah
dicampur dalam air
Cara
Kerjanya : Quats bekerja dengan cara merusak membran sel sehingga terjadi
perubahan permeabilitas membran sel.
Pada kondisi normal, membran sel bersifat permeabel (selektif) terhadap zat-zat
kimia tertentu yang dibutuhkan oleh mikroorganisme.
2.2.5.
Amonium kuartener
Amonium
kuartener merupakan garam ammonium dengan substitusi gugus alkil pada beberapa atau keseluruhan atom H dari ion NH4+nya. Umumnya yang digunakan adalah en:cetyl
trimetil ammonium bromide
(CTAB) atau lauril dimetil benzyl klorida. Amonium kuartener dapat digunakan
untuk mematikan bakteri gram positif, namun kurang efektif terhadap bakteri
gram negatif, kecuali bila ditambahkan dengan sekuenstran (pengikat ion logam).
Senyawa ini mudah berpenetrasi, sehingga cocok diaplikasikan pada permukaan berpori, sifatnya stabil, tidak korosif, memiliki umur simpan panjang, mudah terdispersi, dan menghilangkan bau tidak sedap. Kelemahan dari senyawa ini adalah aktivitas disinfeksi lambat, mahal, dan menghasilkan residu.
Senyawa ini mudah berpenetrasi, sehingga cocok diaplikasikan pada permukaan berpori, sifatnya stabil, tidak korosif, memiliki umur simpan panjang, mudah terdispersi, dan menghilangkan bau tidak sedap. Kelemahan dari senyawa ini adalah aktivitas disinfeksi lambat, mahal, dan menghasilkan residu.
2.2.6.
Kalium permanganat
Kalium
permanganat merupakan zat
oksidan kuat namun tidak tepat untuk disinfeksi air. Penggunaan senyawa ini dapat menimbulkan perubahan
rasa, warna, dan bau pada air. Meskipun begitu, senyawa ini cukup efektif terhadap
bakteri Vibrio
cholerae.
3.
ANTISEPTIK
Antiseptik
atau germisida adalah senyawa kimia yang digunakan untuk membunuh atau
menghambat pertumbuhan mikroorganisme pada jaringan yang hidup seperti pada permukaan kulit dan membran
mukosa. Antiseptik
berbeda dengan antibiotik dan disinfektan, yaitu antibiotik digunakan untuk membunuh mikroorganisme di dalam tubuh, dan disinfektan digunakan untuk membunuh
mikroorganisme pada benda mati.
Hal ini disebabkan antiseptik lebih aman diaplikasikan pada jaringan hidup, daripada disinfektan. Penggunaan disinfektan lebih ditujukan pada benda mati, contohnya wastafel atau meja. Namun, antiseptik yang kuat dan dapat mengiritasi jaringan kemungkinan dapat dialihfungsikan menjadi disinfektan contohnya adalah fenol yang dapat digunakan baik sebagai antiseptik maupun disinfektan.
Penggunaan antiseptik sangat direkomendasikan ketika terjadi epidemi penyakit karena dapat memperlambat penyebaran penyakit.
Hal ini disebabkan antiseptik lebih aman diaplikasikan pada jaringan hidup, daripada disinfektan. Penggunaan disinfektan lebih ditujukan pada benda mati, contohnya wastafel atau meja. Namun, antiseptik yang kuat dan dapat mengiritasi jaringan kemungkinan dapat dialihfungsikan menjadi disinfektan contohnya adalah fenol yang dapat digunakan baik sebagai antiseptik maupun disinfektan.
Penggunaan antiseptik sangat direkomendasikan ketika terjadi epidemi penyakit karena dapat memperlambat penyebaran penyakit.
Efektivitas
antiseptik dalam membunuh mikroorganisme bergantung pada beberapa faktor,
misalnya konsentrasi dan lama paparan. Konsentrasi memengaruhi adsorpsi atau
penyerapan komponen antiseptik.
Pada konsentrasi rendah, beberapa antiseptik menghambat fungsi biokimia membran bakteri, namun tidak akan membunuh bakteri tersebut. Ketika konsentrasi antiseptik tersebut tinggi, komponen antiseptik akan berpenetrasi ke dalam sel dan mengganggu fungsi normal seluler secara luas, termasuk menghambat biosintesis (pembuatan) makromolekul dan persipitasi protein intraseluler dan asam nukleat (DNA atau RNA}. Lama paparan antiseptik dengan banyaknya kerusakan pada sel mikroorganisme berbanding lurus.
Pada konsentrasi rendah, beberapa antiseptik menghambat fungsi biokimia membran bakteri, namun tidak akan membunuh bakteri tersebut. Ketika konsentrasi antiseptik tersebut tinggi, komponen antiseptik akan berpenetrasi ke dalam sel dan mengganggu fungsi normal seluler secara luas, termasuk menghambat biosintesis (pembuatan) makromolekul dan persipitasi protein intraseluler dan asam nukleat (DNA atau RNA}. Lama paparan antiseptik dengan banyaknya kerusakan pada sel mikroorganisme berbanding lurus.
3.1.Jenis – Jenis Antiseptik
Banyak zat kimia yang digolongkan sebagai antiseptik.
Berikut antiseptik yang umumnya digunakan :
- Alkohol 60-90% (etil, atau isopropil, atau ”methylated spirit”).
- Klorheksidin glukonat 2-4% (Hibiclens, Hibiscrub, Hibitane).
- Klorheksidin glukomat dan setrimide, dalam berbagai konsetrasi (Savlon).
- Yodium 3%, yodium dan produk alkohol berisi yodium atau tincture (yodium tinktur).
- Iodofor 7,5-10% berbagai konsentrasi (Betadine atau Wescodyne).
- Kloroksilenol 0,5-4% (para kloro metaksilenol atau PCMX) berbagai konsentrasi (Dettol).
- Triklosan 0,2-2% . (Syaifudin, 2005).
Dalam pemilihan suatu antiseptik, perlu
diperhatikan karakteristik yang diinginkan (misalnya absorpsi dan daya tahan),
keamanan, efektivitas, ketersediaan, penerimaan oleh staf dan yang terpenting
biayanya (Boyce dan Pitter 2002; Larson 1995; Rutala 1996).
Larutan antiseptik yang dianjurkan, aktivitas mikrobiologinya dan potensi penggunaannya. (sistem gradasi yang digunakan pada kolom adalah sangat baik, baik, cukup dan tidak) (Syaifudin, 2005).
Larutan antiseptik yang dianjurkan, aktivitas mikrobiologinya dan potensi penggunaannya. (sistem gradasi yang digunakan pada kolom adalah sangat baik, baik, cukup dan tidak) (Syaifudin, 2005).
3.1.1.
Hidrogen Peroksida (H2O2)
Hidrogen
peroksida (H2O2) adalah cairan bening , agak lebih kental daripada air, yang merupakan oksidator kuat. Sifat terakhir ini dimanfaatkan manusia sebagai
bahan pemutih (bleach), disinfektan, oksidator, dan sebagai bahan bakar roket.
Hidrogen
peroksida dijual bebas, dengan berbagai merek dagang dalam konsentrasi rendah
(3-5%) sebagai pembersih luka atau sebagai pemutih gigi (pada konsentrasi
terukur). Dalam konsentrasi agak tinggi (misalnya merek dagang Glyroxyl®)
dijual sebagai pemutih pakaian dan disinfektan. Penggunaan hidrogen peroksida
dalam kosmetika dan makanan tidak dibenarkan karena zat ini mudah bereaksi
(oksidan kuat) dan korosif.
Sebagai
antiseptik untuk membersihkan debris-debris pada luka lama, bisul dan luka
bernanah. Short acting antiseptic artinya kerja antiseptik ini pendek. Dapat
diaplikasikan sebagai : Wound dressing (hidrogen peroksida 3%), tetes telinga
2%, namun punya rentag efektifitas 3-7%.
Sensitif pada bakteri aerob (gram
positif dan gram negatif). Kurang sensitif pada pyogenic cocci dan spora. Efek
sampingnya adalah iritasi kulit dan mukosa sifatnya sementara.
Cara
kerjanya : Mengoksidasi
komponen-komponen sel mikroorganisme
seperti ; protein, lemak dinding sel dan
asam nukleat. Hampir seluruh bagian sel terpengaruh.Komponen sel yang
teroksidasi mengalami perubahan struktur sehingga tidak berfungsi semestinya.
3.1.2.
Iodine (Golongan
Halogen)
Biasanya
digunakan untuk irigasi intraurine dan vaginal ( ≤ 0.2% ). Iodine tincture USP
mengandung 2% iodine dan 2,4% sodium
iodida dalam alcohol. Antiseptic paling
aktif untuk kulit yang tidak mengalami gangguan, reaksi hipersensitivitas
tinggi dan efek staining.
Cara
Kerja : Oksidasi, Protein, lemak dan asam nuklet bila teroksidasi akan
mengalami parubahan struktur dan tidak berfungsi sebagaimana mestinya. Proses
oksidasi menghasilkan efek yang cepat (< 3 menit) . disarankan lebih baik waktu kontak minimal 10 menit.
3.1.3.
Iodophore (Golongan
Halogen)
Iodophore
adalah persiapan yang mengandung iodine dikomplekskan dengan agen pelarut,
seperti surfaktan atau povidone (membentuk povidone-iodine). Hasilnya adalah
bahan yang larut dalam air yang melepaskan yodium bebasketika dalam larutan.
Iodophors disiapkan oleh pencampuran yodium dengan agen pelarut, panas dapat
digunakan untuk mempercepat reaksi.
Iodophor
sering digunakan oleh pembuat bir dan pembuat anggur untuk membersihkan peralatan
dan botol. Keuntungan utamanya atas pembersih lainnya adalah bahwa ketika
digunakan dalam proporsi yang tepat menguap langsung dari solusi ke gas, dan
karenanya tidak meninggalkan residu. Namun, juga dapat meninggalkan noda
oranye-coklat pada bagian plastik dan
peralatan yang dibiarkan kontak dengan.
Hal
ini sering diberikan dalam konsentrasi yang berbeda dan selanjutnya diencerkan
dengan air sebelum digunakan. Label akan menyarankan rasio pengenceran yang
sesuai, 1:1000 atau 1:100 umumnya. Peralatan yang akan dibersihkan harus
benar-benar bersih dan kiri dalam kontak dengan larutan selama minimal 2 menit.
Iodophore
bisa dikatakan sebagai senyawa komplek iodine dengan agen aktif permukaan
seperti polivinyl pyrrolidone (PVP;povidone-iodine). Iodine berada dalam bentuk
terikat oleh surfaktan dan akan dilepaskan perlahan-lahan saat penggunaan.
Jumlah iodine bebas akan dirilis ketika larutan diencerkan. Iodophore harus diencerkan sesuai petunjuk produsen untuk mendapatkan aktivitas penuh Agen ini mampu membunuh bakteri vegetatif, jamur dan virus yang mengandung lipid. Cara kerjanya adalah sama dengan Iodine.
Jumlah iodine bebas akan dirilis ketika larutan diencerkan. Iodophore harus diencerkan sesuai petunjuk produsen untuk mendapatkan aktivitas penuh Agen ini mampu membunuh bakteri vegetatif, jamur dan virus yang mengandung lipid. Cara kerjanya adalah sama dengan Iodine.
3.1.4.
Clorine
Senyawa
klorin
yang paling aktif adalah asam
hipoklorit. Mekanisme
kerjanya adalah menghambat oksidasi glukosa dalam sel mikroorganisme dengan cara menghambat enzim-enzim yang terlibat dalam metabolisme karbohidrat . Kelebihan dari clorine ini adalah mudah digunakan, dan
jenis mikroorganisme yang dapat dibunuh dengan senyawa ini juga cukup luas,
meliputi bakteri gram positif dan bakteri gram negatif.
Kelemahan dari clorine berbahan dasar klorin adalah dapat menyebabkan korosi pada pH rendah (suasana asam), meskipun sebenarnya pH rendah diperlukan untuk mencapai efektivitas optimum antiseptik ini. Klorin juga cepat terinaktivasi jika terpapar senyawa organik tertentu
Kelemahan dari clorine berbahan dasar klorin adalah dapat menyebabkan korosi pada pH rendah (suasana asam), meskipun sebenarnya pH rendah diperlukan untuk mencapai efektivitas optimum antiseptik ini. Klorin juga cepat terinaktivasi jika terpapar senyawa organik tertentu
Bekerja
sebagai agen oksidasi kuat, bekerja cepat dan spektrum luas, digunakan pada
tempat berventilasi.
Tersedia dalam
bentuk cair dan granul;
a.
Cairan Sodium hipoklorit, 0,5%, 4%, 5-15% klorin (bleach)
b.
Kalsium hipoklorit, 65-70% klorin
c. Bentuk cair stabil pada
konsentrsi maksimal 7% (pada konsentrasi 8-15% bertahan 2 minggu setelah
pembuatan).
d.
Klorin kering lebih stabil pada tempat kering
3.1.5.
Alkohol
Dari
golongan alkohol yang paling sering digunakan sebagai antiseptik adalah alkohol ethanol (70%), methanol (70-80%). Aktivitas alkohol
meningkat dengan bertambahnya panjang rantai pada struktur dan bertambahnya
bobot molekul.
Keuntungannya ; spektrum luas, bekerja cepat, mudah diperoleh, non staining dan tidak menghasilkan residu.
Kerugian : membutuhkan waktu kontak yang lama, mudah menguap yang dapat mengurangi konsentrasi dan mudah terbakar.
Keuntungannya ; spektrum luas, bekerja cepat, mudah diperoleh, non staining dan tidak menghasilkan residu.
Kerugian : membutuhkan waktu kontak yang lama, mudah menguap yang dapat mengurangi konsentrasi dan mudah terbakar.
Cara Kerjanya : melarutkan lipid pada membran sel dan menyebabkan
denaturasi protein mikroorganisme.
Etil dan
isopropil alkohol 60-90% merupakan antiseptik yang baik dan mudah diperoleh
serta murah. Sangat efektif dalam mengurangi mikroorganisme di kulit. Juga
efektif terhadap virus hepatitis dan HIV, jangan dipakai untuk selaput lendir
(misalnya di vagina), karena alkohol mengeringkan dan mengiritasi selaput
lendir dan kemudian merangsang pertumbuhan mikroorganisme.
Menurut Larson (1995) alkohol merupakan
salah satu antiseptik paling aman. Etil atau isopropil alkohol 60-70% efektif
dan pengeringan kulit kurang pada konsentrasi lebih tinggi, lebih murah dari
yang konsentrasi lebih tinggi. Karena pengeringan pada kulit kurang, etil
alkohol lebih sering digunakan pada kulit.
Keuntungan :
- Cepat membunuh jamur dan bakteri termasuk mikrobakteri; isopropil alkohol membunuh sebagian besar virus, termasuk HBV dan HIV; etil alkohol membunuh semua jenis virus.
- Walaupun alkohol tidak mempunyai efek membunuh yang persisten, pengurangan cepat mikroorganisme di kulit, melindungi organisme tumbuh kembali bahkan di bawah sarung tangan selama beberapa jam.
- Relatif murah dan tersedia di mana-mana.
Kerugian :
- Memerlukan emulien (misalnya gliserin dan atau propilen glikol) untuk mencegah pengeringan kulit.
- Mudah pengeringan kulit.
- Mudah diinaktivasi oleh bahan-bahan organik.
- Mudah terbakar sehingga perlu disimpan di tempat dingin atau berventilasi baik.
- Merusak karet atau lateks.
- Tidak dapat dipakai sebagai bahan pembersih. (Syaifudin, 2005)
3.1.6.
Triclosan
Triclosan adalah antiseptik yang efektif dan populer, bisa
ditemui dalam sabun, obat kumur, deodoran, dan lain-lain. Triclosan mempunyai
daya antimikroba dengan spektrum luas (dapat melawan berbagai macam bakteri)
dan mempunyai sifat toksisitas minim. Mekanisme kerja triclosan
adalah dengan menghambat biosintesis lipid sehingga membran mikroba kehilangan kekuatan dan
fungsinya.
Triclosan adalah bahan kimia yang ditambahkan ke
dalam beberapa produk yang berfungsi sebagai antikuman. Triclosan sudah
digunakan sejak 40 tahun yang lalu. Mula mula, triclosan digunakan di rumah
sakit sebagai bahan antikuman. Penggunaan pada produk rumah tangga baru
dilakukan secara meluas sejak 15 tahun yang lalu.
Badan pengawas obat dan makanan Amerika Serikat atau FDA saat ini
sedang meneliti efek berbahaya dari triclosan. Banyak yang beranggapan bahwa
triclosan bertanggung jawab atas pencemaran air minum di Amerika dan efek
resistensi kuman terhadap antibiotika. Meskipun FDA tetap beranggapan bahwa
triclosan aman digunakan pada manusia, tetapi penelitian tentang efek berbahaya
dari triclosan masih terus berlangsung.
Penentang keputusan FDA tentang keamanan triclosan beranggapan bahwa
pada penelitian terhadap binatang percobaan, triclosan menganggu hormon yang
berfungsi pada pertumbuhan otak dan alat reproduksi. Gangguan ini akan menyebabkan
seseorang kesulitan dalam belajar dan mandul. Selain itu, triclosan
juga diduga bertanggung jawab atas maraknya resistensi kuman terhadap antibiotika.
Triklosan adalah subtansi tidak berwarna yang terdapat dalam
sabun sebagai antimikrobial. Konsentrasi 0,2-2,0% mempunyai aktivitas
antimikrobial sedang terhadap koki gram positif, mikobakteria dan jamur, tapi
tidak terhadap baksil gram negatif, khususnya P aeruginosa (Larson 1995).
Meskipun perhatian ditujukan pada resistensi terhadap bahan ini bisa berkembang
lebih siap dari bahan antiseptik lain, resistensi pada flora kulit tidak
ditemukan penelitian klinis sampai saat ini.
Keuntungan :
- Aktivitas berspektrum luas.
- Persistensi sangat bagus.
- Sedikit efeknya oleh bahan organik.
Kerugian :
- Tidak ada efeknya terhadap P aeruginosa atau baksil gram negatif lain.
- Bakteriostatik (hanya mencegah pertumbuhan). (Syaifudin, 2005)
3.1.7.
Asam Borat (Boraks)
Asam Borat merupakan antiseptik lemah, tidak
mengiritasi jaringan. Zat ini dapat digunakan secara optimum saat dilarutkan
dalam air dengan perbandingan 1:20.
Boraks merupakan garam natrium yang banyak digunakan di berbagai
industri nonpangan, khususnya industri kertas, gelas, pengawet kayu, dan
keramik. Ia tidak berwarna dan gampang larut dalam air. Gelas pyrex yang terkenal kuat bisa memiliki
performa seperti itu karena dibuat dengan campuran boraks. Kemungkinan besar
daya pengawet boraks disebabkan oleh senyawa aktif asam borat.
Asam borat (H3BO3) merupakan asam organik lemah
yang sering digunakan sebagai antiseptik, dan dapat dibuat dengan menambahkan
asam sulfat (H2SO4) atau asam khlorida (HCl) pada boraks.
Asam borat juga sering digunakan dalam dunia pengobatan dan kosmetika.
Misalnya, larutan asam borat dalam air (3%) digunakan sebagai obat cuci mata dan dikenal sebagai boorwater. Asam borat juga digunakan sebagai obat kumur, semprot hidung, dan salep luka kecil. Namun, ingat, bahan ini tidak boleh diminum atau digunakan pada luka luas, karena beracun ketika terserap masuk dalam tubuh.
Misalnya, larutan asam borat dalam air (3%) digunakan sebagai obat cuci mata dan dikenal sebagai boorwater. Asam borat juga digunakan sebagai obat kumur, semprot hidung, dan salep luka kecil. Namun, ingat, bahan ini tidak boleh diminum atau digunakan pada luka luas, karena beracun ketika terserap masuk dalam tubuh.
3.1.8.
Garam Merkuri
Senyawa ini adalah antiseptik yang paling kuat. Merkuri klorida (HgCl) dapat digunakan untuk mencuci tangan
dengan perbandingan dalam air 1:1000.. Senyawa ini dapat membunuh hampir semua
jenis bakteri dalam beberapa menit.. Kelemahan dari senyawa ini adalah
berkemungkinan besar mengiritasi jaringan karena daya kerja antimikrobanya yang
sangat kuat.
3.1.9.
Klorheksidin
Glukonat (CHG)
Klorheksidin glukonat adalah antiseptik yang sangat baik. Ia
tetap aktif terhadap mikroorganisme di kulit beberapa jam sesudah pemberian dan
aman bahkan untuk bayi dan anak. Karena klorheksidin glukonat diinaktivasi oleh
sabun, aktivitas residualnya bergantung pada konsentrasinya. Konsentrasi 2-4%
merupakan yang dianjurkan. Formulasi baru 2% dalam air dan 1% klorheksidin
tanpa air, dicampur alkohol juga efektif.
Keuntungan :
- Antimikrobial spektrum luas.
- Secara kimiawi aktif paling sedikit 6 jam.
- Perlindungan kimiawi (jumlah mikroorganisme terhalang) meningkat dengan penggunaan ulang.
- Pengaruh material organik minimal.
- Tersedia produk komersial, yang umum adalah dicampur dengan deterjen dan alkohol.
Kerugian :
- Mahal dan tidak selalu tersedia.
- Efek dikurangi atau dinetrelisasi oleh sabun, air ledeng, dan beberapa krim tangan.
- Tidak efektif terhadap basil TBC, baik dan efektif melawan jamur.
- Tidak dapat dipakai pada pH > 8 karena mengalami dekomposisi.
- Hindari kontak dengan mata, karena dapat mengakibatkan konjungtivitas. (Syaifudin, 2005)
3.1.10.
Kloroheksilenol
Kloroheksilenol (para-kloro-metaksilenol atau PCMX) adalah
devisi halogen dari silenol yang luas tersedia dalam konsentrasi 0,5-4%.
Kloroheksilenol memecahkan mikroorganisme dengan memecah dinding sel. Hal ini
merupakan penghapus kuman yang beraktivitas rendah (Fevero, 1985) dibandingkan
dengan alkohol, yodium, iodofor dan kurang efektif dalam menurunkan flora kulit
daripada CHG atau iodofor (Sheen dan Stiles, 1982).
Karena ia menembus kulit, dapat beracun jika dioleskan pada beberapa bagian dari tubuh, dan tidak boleh digunakan pada bayi. Meskipun, produk komersil dengan kloroheksilenol dengan konsentrasi di atas 4% tidak boleh digunakan.
Karena ia menembus kulit, dapat beracun jika dioleskan pada beberapa bagian dari tubuh, dan tidak boleh digunakan pada bayi. Meskipun, produk komersil dengan kloroheksilenol dengan konsentrasi di atas 4% tidak boleh digunakan.
Keuntungan :
- Aktivitas bersepektrum luas.
- Hanya sedikit efeknya terhadap materi organik.
- Efek residu tahan sampai beberapa jam.
- Minimal efek oleh bahan organik.
Kerugian :
- Diinaktivasi oleh sabun (surfaktan nonionik), penggunaan untuk persiapan kulit berkurang.
- Tidak boleh digunakan pada bayi baru lahir, karena dapat menyerap dengan cepat dan potensial meracuni. (Syaifudin, 2005)
Sterilisasi
Sterilisasi merupakan proses mematikan semua organisme
termasuk bakteri- bakteri,spora bakteri,kapang dan virus,secara kimia atau
secara fisika serta mencegah organisme tersebut agar tidak kembali hidup.
Metode- metode sterilisasi :
A.Metode sterilisasi
panas
Penguapan
bertekanan tinggi yang menggunakan autoklaf atau pemanasan kering dengan oven.
Sterilisasi
uap tekanan tinggi :
Metode
sterilisasi yang efektif untuk mensterilkan instrumen dan alat- alat lain yang
digunakan pada berbagai fasilitas pelayanan
kesehatan. Contoh, autokalf
Sterilisasi
panas kering (oven) :
Membutuhkan
listrik terus-menerus, kurang efektif di daerah terpencil,digunakan pada
benda-benda gelas atau logam,karena akan melelehkan bahan lainnya.
B.Sterilisasi dengan cara penguapan
Penguapan
adalah sterilan yang efektif karena 2 alasan yaitu :
Pertama,uap pekat adalah sebuah kendaraan energi termal yang sangat efektif. Kedua,uap adalah sterilan yang efektif karena lapisan luar mikroorganisme bersifat protektif dan resistan dapat dilemahkan oleh uap,sehingga terjadi koagulasi pada bagian mikroorganisme yang sensitif.
Kelebihan
Paling efektif ,waktu sterilisasi lebih pendek daripada
panas kering atau siklus kimia.
Kekurangan
Membutuhkan
sumber panas yang terus-menerus, membutuhkan peralatan yang butuh perawatan
serius, bahan plastik tidak tahan suhu tinggi.
C.Sterilisasi kimia
Digunakan
apabila dengan sterilisasi panas kering atau sterilisasi tekanan tinggi akan
merusak objek tersebut atau peralatan tidak tersedia.
Kelebihan
Larutan
glutyaraldehid dan formaldehid tidak begitu mudah dinonaktifkan oleh materi
organik, kedua larutan ini digunakan untuk instrumen yang tidak tahan
sterilisasi panas,seperti
leparoskop
Kekurangan
Glutaraldehid
mahal harganya. Formaldehid tidak dapat dicampur dengan clorin karena
memproduksi gas berbahaya.
Macam-macam sterilasasi :
Pada
prinsipnya sterilisasi dapat dilakukan dengan 3 cara yaitu secara mekanik,
fisik dan kimiawi.
- Sterilisasi secara mekanik (filtrasi) menggunakan suatu saringan yang berpori sangat kecil (0,22 mikron atau 0,45 mikron) sehingga mikroba tertahan pada saringan tersebut. Proses ini ditujukan untuk sterilisasi bahan yang peka panas, misalnya larutan enzim dan antibiotic.
- Sterilisasi secara fisik dapat dilakukan dengan pemanasan dan penyinaran.
- Pemanasan
- Pemijaran (dengan api langsung) : membakar alat pada api secara langsung, contoh alat : jarum inokulum, pinset, batang L.
- Panas kering : sterilisasi dengan oven kira-kira 60-1800 C. sterilisasi panas kering cocok untuk alat yang terbuat dari kaca misalnya Erlenmeyer, tabung reaksi.
- Uap air panas : konsep ini mirip dengan mengukus. Bahan yang mengandung air lebih tepat menggunakan metode ini supaya tidak terjadi dehidrasi
- Uap air panas bertekanan : menggunakan autoklaf
- Penyinaran dengan UV
Sunar ultra
violet juga dapat digunakan untuk proses sterilisasi, misalnya untuk membunuh
mikroba yang menempel pada permukaan interior safety cabinet dengan disinari
lampu UV.
- Sterilisasi secara kimiawi
biasanya menggunakan senyawa
desinfektan seperti yang dijelaskan sebelumya.
Sterilisasi dengan penyaringan (filtrasi)
Sterilisasi dengan penyaringan (filtrasi)
Sterilisasi
dengan penyaringan dilakukan untuk mensterilisasi cairan yang mudah rusak jika
terkena panas atau mudah menguap (volatile).
Cairan yang
disterilisasi dilewatkan kesuatu saringan (ditekan dengan gaya setrifugasi atau
pompa vakum) yang berpori dengan diameter yang cukup kecil untuk menyaring
bakteri. Virus tidak akan tersaring dengan metode ini.
- Sterilkan saringan (dapat menggunakan saringan bekerfeld, chamberland zitz), membrane penyaring (kertas saring) dan Erlenmeyer penampung.
- Pasang atau rakit alat-alat tersebut secara aseptis (sesuai gambar), lalu isi corong dengan larutan yang akan disterilkan.
- Hubungkan katup Erlenmeyer dengan pompa vakum kemudian hidupkan pompa
- Setelah semua larutan melewati membrane filter dan tertampung dierlenmeyer, maka larutan dapat dipindahkan kedalam gelas penampung lain yang steril dan tutup dengan kapas atau alumunium foil yang steril.
Sterilisasi dengan udara panas (dry heat sterilization)
Sterilisasi
dengan metode ini biasanya digunakan untuk peralatan gelas seperti cawan petri,
pipet ukur dan labu Erlenmeyer.
Alat gelas
yang disterilisasi dengan udara panas tidak akan timbul kondensasi sehingga
tidak ada tetes air (embun) didalam alat gelas.
- Bungkus alat-alat gelas dengan kertas peyung atau alumunium foil
- Atur pengatur suhu oven menjadi 1800 C dan alat disterilkan selama 2-3 jam.
4.
PERBEDAAN STERILISASI
DAN DISINFEKSI
Sterilisasi
1.
Semua mikroba termasuk spora bakteri akan terbunuh.
- Dapat dilakukan dengan menggunakan pemanasan uap (autoklav) atau dengan panas kering.
- Dapat juga dilakukan dengan penjenuhan dengan glutaraldehid atau formaldehid selama 10 jam.
Desinfeksi
tingkat tinggi
- Semua mikroba, sebagian dari spora bakteri terbunuh.
- Dapat dilakukan dengan pendidihan selama 20 menit atau dengan penjenuhan dengan jumlah besar disinfektan selama 30 menit misalnya dengan mengunakan glutaraldehid atau H2O2
Desinfeksi
tingkat rendah
Akan menghilangkan jumlah mikroba
sehingga peralatan atau permukaan badan aman untuk dipegang. Desinfeksi ini
dapat dilakukan dengan beberapa macam disinfektan(Signaterdadie, 2009)
DAFTAR PUSTAKA
Anonimous. 2007. Pasteurisasi. http://ptp2007.wordpress.com/category/pasteurisasi.
diakses tanggal 8 Oktober 2011.
Kustiningsih, Heris. 2010. Susu Pasteurisasi. http://www.deptan.go.id/bpsdm/bbpkh_cinagara/index.php?option=com_content&view=article&id=66:susu&catid=32:kesmavet&Itemid=47.
Diakses tanggal 8 Oktober 2011.
Mulyani, Diyah Yuyun Sri. 2008. Uji Organoleptik Dan Kadar Vitamin C Dodol
Susu Pasteurisasi Dengan Penambahan Ekstrak Lidah Buaya (Aloe Vera). Skripsi. Surakarta:
Universitas Muhammadiyah Surakarta
Rahardjo, Pratolo.2010. Sistem Pengendali Temperatur Untuk Proses
Pasteurisasi Alat-Alat Medis.Bukit Jimbaran: Fakultas Teknik, Unud. Vol. 9 No.1.
Staff Farmakologi.2011.Disinfektan dan Antiseptik.Denpasar:Fakultas Kedokteran Hewan Universitas Udayana.
Suparyanto. 2010. Konsep Disinfektan. http//:.suparyanto.com. diakses tanggal 8 Oktober 2011
Susiani. 2007. Boraks Ada Dalam Makanan Kita. Fakultas MIPA Undip-32 : http://www.suaramerdeka.com/harian. Diakses tanggal 8 Oktober 2011.
Syabatini, Annisa. 2009. Kinetika Reaksi Hidrogen Peroksida Dan Asam Iodida. Banjarbaru :Universitas Lambung Mangkurat. http://annisanfushie.wordpress.com. Diakses tanggal 8 Oktober 2011.
SyamsirPrinsip Pasteurisasi dan Sterilisasi Komersial Produk Pangan. http://id.shvoong.com/tags/pasteurisasi. diakses tanggal 8 Oktober 2011.
Wikipedia.2011.Antiseptik. http://id.wikipedia.org/wiki/Antiseptik. diakses tanggal 8 Oktober 2011.
Wikipedia.2011.Disinfektan. http://id.wikipedia.org/wiki/Disinfektan. diakses tanggal 8 Oktober 2011.
Wikipedia.2011.Hidrogen Peroksida. http://id.wikipedia.org/wiki/Hidrogen-Peroksida. diakses tanggal 8 Oktober 2011.
Wikipedia.2011.Iodophor. http://eng.wikipedia.org/wiki/Iodophor. diakses tanggal 8 Oktober 2011.
Wikipedia.2011.Formaldehyde. http://eng.wikipedia.org/wiki/Formaldehyde. diakses tanggal 8 Oktober 2011.
Wikipedia.2011.Pasteurisasi. http://id.wikipedia.org/wiki/pasteurisasi. diakses tanggal 8 Oktober 2011.
Wirawan, I Made Cock. 2010. Keamanan Triclosan Dipertanyakan. http://www.blogdokter.net/2010/04/14/keamanan-triclosan-dipertanyakan.
diakses tanggal 8 Oktober 2011
Pasteurisasi, Desinfeksi, dan Sterilisasi
 Reviewed by kangmaruf
on
12:09 AM
Rating:
Reviewed by kangmaruf
on
12:09 AM
Rating:
 Reviewed by kangmaruf
on
12:09 AM
Rating:
Reviewed by kangmaruf
on
12:09 AM
Rating:
























No comments: